Introduction
고빌리루빈혈증은 신생아기에 가장 흔히 볼 수 있는 질환으로 전세계적으로 생후 일주일내 신생아 중 약 80%에서 관찰된다(Stoll and Kliegman, 2004). 생리학적 비접합 고빌리루빈혈증이 발생하는 것으로 대부분 일시적이고 양호한 결과를 나타내지만 심각하게 발전하여 고빌리루빈혈증으로 고통받는 신생아가 전세계적으로 약 100만명에 이른다. 고빌리루빈혈증을 치료하지 않을 경우 핵황달 및 사망에 이르는데, 매년 120,000명의 아기가 황달로 사망하고 더 많은 사람들이 영구적인 신경 손상(kernicterus)으로 고통받고 있다. 이러한 사망의 대부분은 사하라 사막 이남의 아프리카와 남아시아의 저소득 국가에서 발생한다(Bhutani et al., 2013; Bolajoko et al., 2018). 따라서 신생아 고빌리루빈혈증, 특히 핵황달의 발생의 위험성을 줄이기 위해서는 의료환경이 열악한 환경에서도 사용할 수 있도록 가격이 저렴하고 신속하고 정확하게 진단할 수 있는 현장진단법의 개발이 매우 중요하다.
총빌리루빈을 측정하기위해 임상 실험실에서는 주로 diazo 방법으로 아조빌리루빈을 생성하여 분광광도계로 측정하고 있으며 자동화 장비를 사용한다(Sykes and Epstein, 1990; Doumas and Wu, 1991). 검사의 정확도는 높으나 일정량의 피를 채혈하여야 하고 고가의 장비 및 전문인력이 필요하며 현장에서 측정이 불가능하기 때문에 심각한 고빌리루빈혈증이 있는 경우 치료가 지연될 수 있다. 따라서 현장 진료(POC)가 가능한 제품으로 직접 분광광도법 및 경피적 빌리루빈미터가 개발되었다.
기존의 방법과 비교할 때 현장 진료(POC) 직접 분광 광도법에 의한 총빌리루빈 측정은 혈액 샘플 요구량이 적고 처리 시간이 더 빠른 장점이 있다. 혈청 샘플 20 ul를 장치에 넣고 15초 이내 결과를 확인할 수 있으며 HPLC 결과와 비교시에도 상관관계가 0.99로 높다고 알려져 있다(Kazmierczak et al., 2002; Barko et al., 2006) 그러나 별도의 원심분리기를 이용한 혈청 분리가 필요하여 과정이 복잡하고 현장 어디서나 사용할 수 없다.
경피적 빌리루빈미터는 스펙트럼 반사율을 사용하여 피부와 피하 조직의 빌리루빈(발색단)의 양을 결정하며, 이는 총빌리루빈 농도와 상관 관계를 이용하여 추정치를 제공한다. 경피적 방법은 영아에서 수행되는 발뒤꿈치 채혈에 대한 부담을 줄여주고, 즉각적인 결과와 사용 용이성 등의 이점이 있다. 경피적 측정법과 혈청검사는 0.7에서 0.97사이의 상관계수를 나타내어 선별검사로 사용하고 있지만(Willems et al., 2004; Chokemungmeepisarn et al., 2020; Cucuy et al., 2018) 인종, 광선치료, 재태주수, 측정부위에 따라 영향을 받는다는 단점이 있다. 최근 2개의 파장 대역을 활용 및 측정 알고리즘 개선으로 측정부위 및 피부톤의 영향을 줄여 정확도가 향상된 제품이 보편적으로 사용되고 있으나 여전히 매우 밝거나 어두운 피부톤이나 피부의 상태에 영향을 받는다(Arman et al., 2020; 노의정 외, 2006).
따라서 의료시설이 열악한 환경에서 누구나 간편하게 검사할 수 있고, 사용자에 의한 변이 요인이 없이 빌리루빈을 측정할 수 있는 제품의 개발이 요구된다. 본 연구에서는 일상 생활에서 보편적으로 사용하는 스마트폰을 이용한 빌리루빈 측정기기를 개발을 통해 현장에서 신속하게 신생아의 혈청 빌리루빈 결과를 얻어서 영유아의 황달 상태 파악 및 치료방침을 결정하는데 기여하고자 한다.
Theory
1. 측정원리
총 빌리루빈의 측정 원리는 변형된 Jendrassik and Grof 방법(Damjanow, 2009; Lo and Wu, 1983)으로 bilirubin에 diazo 시약을 부착시켜 붉은색의 azobilirubin으로 변형시킨 후 발색 반응을 통해 빌리루빈 수치를 측정한다(Figure 1).
결합형 빌리루빈은 diazo와 직접 반응하지만 비결합형 빌리루빈은 dyphylline과 먼저 반응하여 diazo 반응을 촉진시켜야 한다. 혈액을 떨어뜨리면 분리 패드에서 dyphylline에 의해 비결합형 빌리루빈을 결합형 빌리루빈 형태로 변화시키고, 결합 빌리루빈은 2,4-dichlorobenzenediazonium salt와 반응하여 디아조염을 형성하고 Red 계열로 발색을 하게 된다.
Materials and Methods
1. Materials
본 연구에 사용한 임상검체는 장원의료재단의 IRB(Internal Review Board)의 승인을 받아 ethylenediaminetetraacetic acid (EDTA)가 처리된 정맥혈을 사용하였다. 시스템 정확도를 분석하기 위해 Table 1과 같이 7구간의 농도 검체를 사용하였으며, 잔여검체수집이어려운고농도검체의경우 Bilirubin stock 용액을 이용하여 조제혈을 만들어 사용하였다.
Cobas c 111 임상화학 분석기(Roche Diagnostics Corp. Germany)를 기준장비로 사용했다. 비교 장비로는 BR-5200 (APEL Co, Japan)를 사용했다.
2. Methods
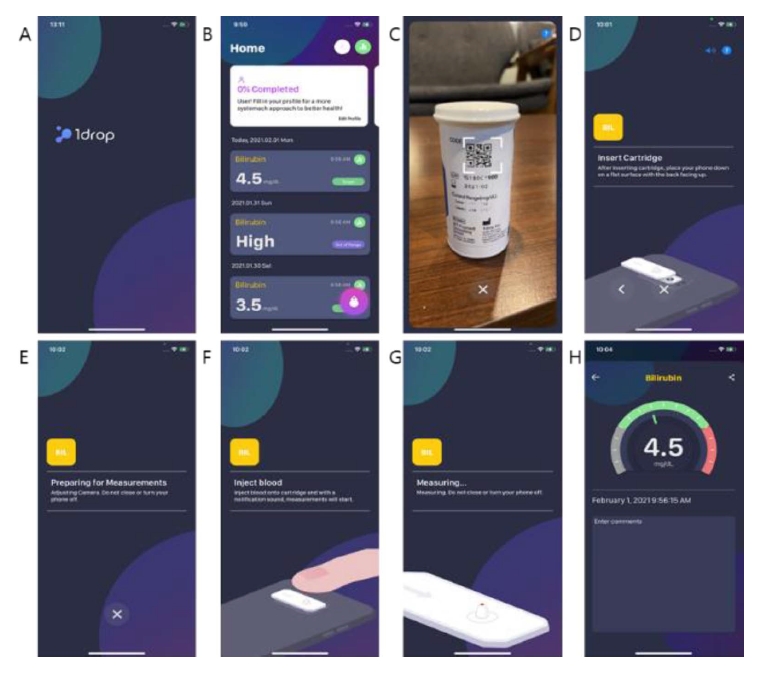
스마트폰을 이용한 총빌리루빈 측정시스템의 측정방법은 Figure 2와 같다. 스마트폰의 전용 어플리케이션을 실행하고 QR 코드를 통해 카트리지 정보를 읽는다. 카트리지를 커버에 고정시키면 calibration이 진행되고 안내에 따라 전혈 5 ul를 점적한다. 혈액주입이 확인되면 측정이 시작되고 1분 내 표시된 결과값을 확인한다.
기준장비(Cobas c111, Roche Diagnostics Corp. Germany)과 비교장비(BR-5200, APEL CO., KTD, Japan)는 사용자설명서에 따라 전혈에서 혈장을 분리하여 측정하였다.
Results and Discussion
1. 스마트폰을 이용한 총빌리루빈 측정 시스템의 설계
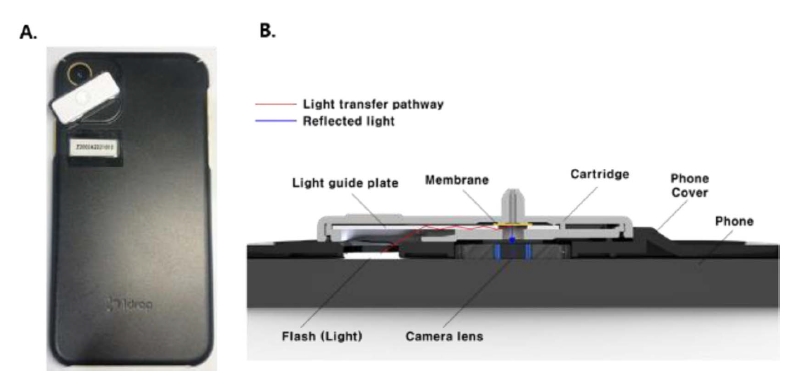
스마트폰을 이용한 측정시스템은 상용 스마트폰과 전용 백커버, 측정 카트리지, 전용 앱으로 구성된다(Figure 3). 측정카트리지는 LED의 빛을 측정영역으로 전달하는 도광판과, 혈구분리와 diazo 반응시약이 건조되어 발색반응이 일어나는 2개의 멤브레인으로 구성되어 있다.
측정 카트리지의 하부 하우징에는 외부 광 유입을 위한광 유입구 및 시료의 반응을 촬영하기 위한 촬영구가 포함된다. 카트리지를 스마트폰 커버에 고정하고 측정부위를 카메라에 위치하게 되고 측정이 시작되면 LED가 켜지고, LED에서 나오는 빛이 카트리지의 도광판을 통해 측정부위로 전달하여 촬영구에서 스마트폰의 카메라는 비색반응에 의한 RGB 값을 얻는다(Figure 4).
2. 발색 반응 및 RGB 측정
센서 스트립에 혈액 5 ul를 떨어뜨리면 혈구분리패드를 거쳐 Diazo 시약이 도포된 멤브레인으로 혈장이 이동하여 발색반응이 일어난다(Figure 5). 혈액이 점적시 RGB 변화에 의해 혈액 주입을 인식할 수 있으며 혈구 분리패드에서 혈장이 분리되면 발색정도에 따라 RGB signal이 변하게 된다. Diazo 시약과 반응하여 붉은색 발색이 일어나기 때문에 농도에 따른 G 값의 상관관계를 이용하여 알고리즘을 도출하여 총빌리루빈 값을 수치적으로 산출하였다.
3. 시스템 정확도
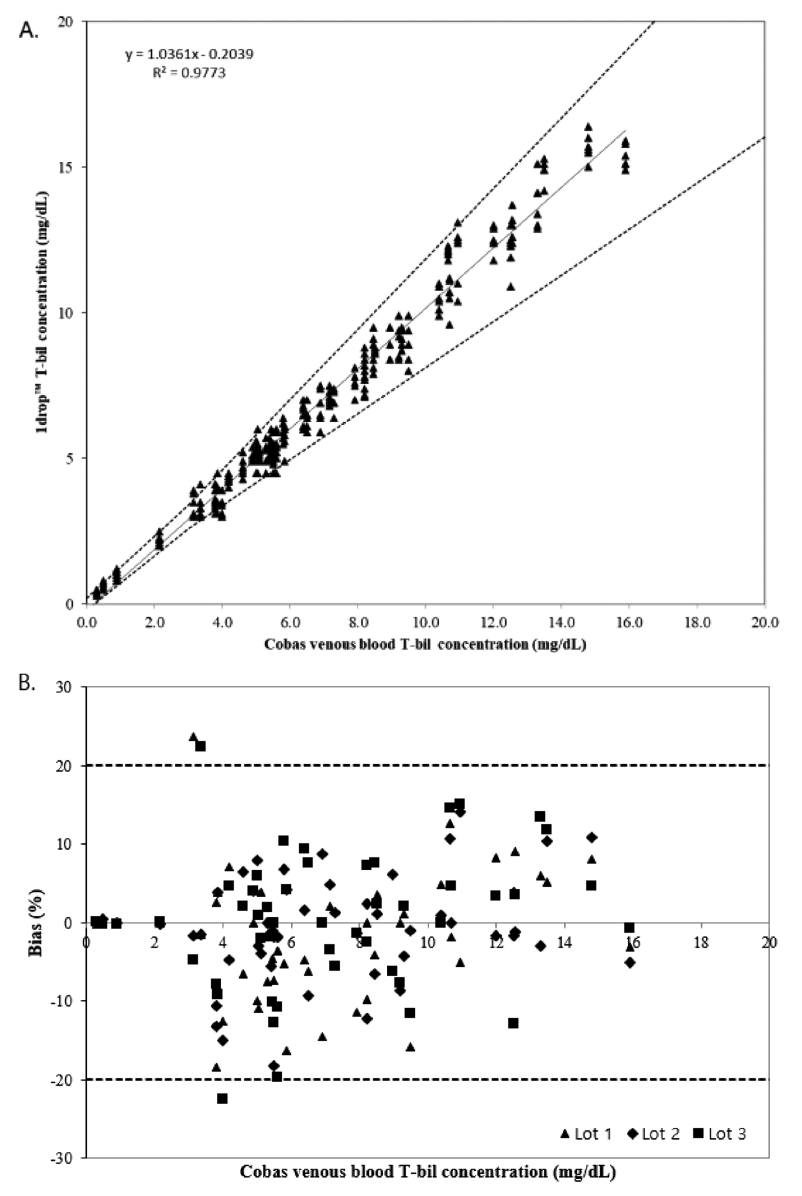
측정 시스템의 정확도를 확인하기 위해 기준장비(Cobas c 111)의 결과값을 기준으로 총빌리루빈 0.3~15.9 mg/dL 농도 구간의 정맥혈 50개 샘플을 측정하였다. 카트리지 3 Lot을 2회 반복 측정하여 총 3 00개 결과를 분석한 결과 기준 장비(Cobas c 111)와의 상관계수(R2)는 0.9769으로 높은 상관관계를 확인했다(Figure 6(A)). 3 mg/dL 이하 농도에서 기준장비 결과값 대비 ±0.4 mg/dL 이내 94%(17/18), 3 mg/dL 이상 농도에서 기준장비 결과값 대비 ±20% 이내 98%(276/282)의 정확도를 확인하였다(Figure 6(B)).
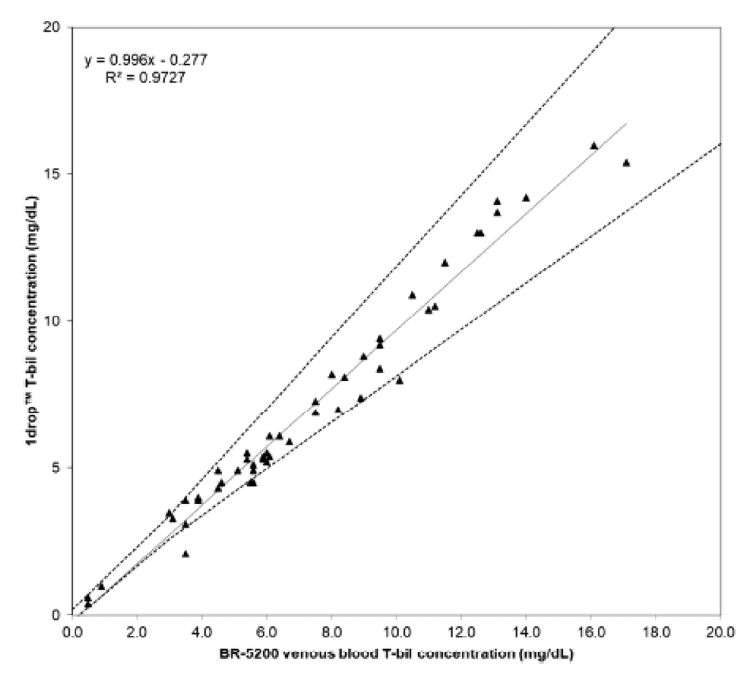
또한 빌리루빈 측정기(BR-5200)의 결과값을 비교한 결과에서도 상관계수(R2)는 0.9727로 높은 상관관계를 보였다(Figure 7).
4. 반복 측정성
측정값의 반복 측정성을 확인하기 위해 0.9, 5.2, 12.1 mg/dL 농도의 혈액을 10회 반복 측정하였다(Table 2). T-bil 측정 시스템의 10회 반복 측정 평균은 1.0, 4.5, 12.4 mg/dL이며 각각의 표준편차는 0.223, 0.192, 0.561이며 3 mg/dL 이상 농도의 CV%는 4.3 %, 4.5%로 확인하였다.
Conclusions
시기 적절한 선별, 치료 및 관리는 신생아 고빌리루빈혈증, 특히 핵황달의 발생의 위험성을 예방할 수 있다. 그러나 저소득 및 중간 소득 국가에서는 의료 시스템이 직면한 문제 때문에 이것이 불가능한 경우가 많다. 의료 시설과의 거리, 훈련된 인력 부족, 부적절한 기반 시설은 모두 진단을 지연시킬 수 있다. 현장진단형 검사는 환자 치료 장소 근처에서 수행되는 검사로 환자 치료에 대한 즉각적인 결정과 변경을 가능하게 한다. 이러한 시기적절한 검사와 진단은 수많은 생명을 구할 수 있다. 따라서 소량의 혈액량을 사용하여 쉽고 간단하게 고빌리루빈혈증을 확인할 수 있는 저렴하며 표준화된 검사 장비가 필요하다. 이 방법은 사용하기 쉽고 빠르며 장비가 필요 없고 필요한 사람들이 쉽게 접근할 수 있어야 한다.
본 연구에서는 상용 스마트폰을 사용하여 편리하고 휴대가 편리한 총빌리루빈 측정시스템을 개발하였다. 이는 전용 커버와 빛 전달 구조의 카트리지를 이용하여 추가의 장치가 필요없이 스마트폰의 LED와 카메라를 이용하여 측정할 수 있기 때문에 현장에서 사용하기 편리하며, 원심분리 등 전처리 과정이 없이 5 ul의 소량의 혈액을 주입하면 되므로 의료전문가가 아니어도 측정이 가능하다.
검사실에서 사용하는 cobas c111의 측정값과 휴대폰 측정 시스템의 값과 비교한 결과 3 mg/dL이하 농도 ±0.4 mg/dL 이내 94%(17/18), 3 mg/dL 이상 농도에서 기준장비 결과값 대비 ±20% 이내 98%(276/282)의 정확도를 확인하였다. 이로써 Clinical Laboratory Improvement Amendments (CLIA) guidelines의 기준 ±20% or 0.4 mg/dL 이내 95%의 이내의 기준을 만족함을 확인하여 고빌리루빈혈증을 측정하는 현장진단제품으로 사용 가능성을 확인하였다. 따라서 신생아 황달선별법으로 적정한 기술로 판단되나 영유아의 임상적 유효성에 대한 연구 평가가 이루어지지 않아 앞으로 지속적인 연구가 필요할 것으로 생각된다.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print